8月7日,陕西省公共资源交易中心发布通知,公示马来酸依那普利片等5个品种7个品规的通过一致性评价仿制药限价情况。
一致性评价“限价”已经来了。

8月7日,陕西省公共资源交易中心发布通知,公示马来酸依那普利片等5个品种7个品规的通过一致性评价仿制药限价情况。
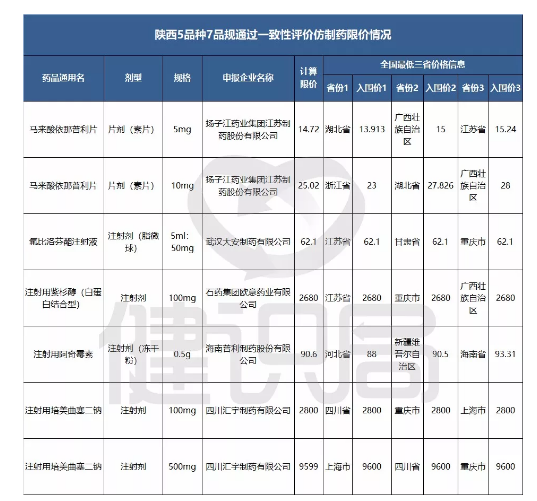
公示期2018年8月7日至8月13日17时,其间无申诉和投诉的产品限价,视作申报人已确认该限价,公示结束后优先挂网公布;有异议的需现场实名递交书面申诉或投诉。
业内人士注意到,陕西省的限价参考了该品种在全国挂网价最低的3省情况。
这意味着,在原研药“降价潮”汹涌而至的同时,其替代产品——通过一致性评价的仿制药也面临采购限价。
化解尴尬?
通过一致性评价仿制药与原研药同组竞争
就在上周五(8月3日),北京、上海、天津、重庆、辽宁、广东、福建、四川、陕西等多省药品招采行政部门参与的药品集中采购试点座谈会上,相关部门刚刚提出“用各省70%的市场份额交换通过一致性评价产品以及原研产品的最低报价,并此产品的最低报价作为医保的支付价”的方案。
分析人士认为,这意味着通过一致性评价药品终于可以与原研药同组竞争,此前困扰企业的“唯低价是取”问题或可化解。
自去年年底,第一批通过一致性评价仿制药名单公示以来,国家食药监管总局药品审评中心(CDE)已先后公示五批,41个品种57个品规通过一致性评价仿制药。此外,《中国药品目录集》和企业公开信息,海南双成药业的注射用胸腺法新,四川汇宇制药的注射用培美曲塞二钠,海南普利制药的注射用阿奇霉素、注射用半托拉唑等注射剂也已通过一致性评价。
此后,这些仿制药直接挂网、临床替代原研药等工作也在加速推进。但,在集中采购环节,这些通过一致性评价的仿制药遭遇了“唯低价是取”的尴尬。从各省发文看,包括陕西在内的至少13个省份发文,要求相关企业提交“全国最低价承诺书”。(详见>>倒计时8个月!仿制药一致性评价仍遭药品集采“最低价”挑战)
未来通过一致性评价的仿制药与原研药共同竞争具体省份的70%市场份额,一方面摆脱了与普通仿制药竞价的尴尬;另一方面,以更高的性价比,在医保支付标准的“筛选”下,结合总额预付下的医保支付方式改革,以及医疗机构的控费压力,通过一致性评价的仿制药无疑将成为医疗机构的首选,赢得真正的利好。
只是底线
压低通过一致性评价品种仍是趋势
虽然,有分析人士认为,国家医保部门此次将通过一致性评价仿制药与原研药放在一起议价,其目的主要是为了实现仿制药的临床替代,但也有专家指出,通过一致性评价只是底线,“只是让企业活下来,别指望能卖高价”。
我国是仿制药大国,据统计全国近20万张上市许可证中,90%以上为仿制药。从产值上看,中国医药工业信息中心数据显示,2016年我国仿制药市场规模约为9167亿元;受慢性病患病率逐年增加、人口老龄化、医保控费等因素影响,预计到2020年,有望达到14116亿元。
但同时,我国并不是仿制药强国。由于历史和现实原因,本土仿制药质量参差不齐,长期面临“安全、无效”的尴尬,与原研药相比差距较大。而这也导致很多进口专利药,虽然过了专利期仍然保持高价位。
因而,为了提高中国仿制药质量并减轻患者用药负担,2015年,国务院印发《关于改革药品医疗器械审评审批制度的意见》,拉开仿制药一致性评价的序幕。
2016年2月,国务院办公厅发布《关于开展仿制药质量和疗效一致性评价的意见》,明确目标——《基本药物目录》(2012年版)中2007年10月1日前批准上市的化学药品仿制药口服固体制剂共289个品种,在2018年底前完成一致性评价。并明确“通过仿制药质量与疗效一致性评价生产企业达到3家以上的,明确不再选用未通过一致性评价的品种”。
虽然,到目前距离最后期限只有不到半年时间,289个品种仍有大半没有通过一致性评价,但相应的利好政策——直接挂网、临床替代等,已在落实。
分析人士表示,虽然一致性评价过程中花费巨大——每个品种近千万,但,通过一致性评价只是“还欠账”。此次陕西省给出限价也是为本土企业敲响警钟,真正的利好还需要通过不断提高生产工艺,加强创新研发投入,提高产品质量来实现。
以上就是仿制药一致性评价机构-桐晖药业小编分享的来自“健识局 ”的有关“通过一致性评价品种限价!参考全国最低价,接受可优先挂网!”的全部内容,供大家参考!
广州市桐晖药业有限公司是一家符合现代化管理要求的GSP公司,在进口原料药细分领域是为业界翘楚,为客户提供专业的从药学研发、临床预BE到临床BE的药厂研发一站式解决方案。目前的重点业务主要包括:原料药联合申报、参比制剂一次性进口、临床预BE/正式BE和一致性评价服务。如需合作,欢迎来电咨询!